[충청뉴스 이성현 기자] 국내 연구진이 시냅스 단백질 속 유전자 조각이 뇌 회로를 조절하는 원리를 규명했다.
기초과학연구원(IBS)은 시냅스 뇌질환 연구단 김은준 연구단장 연구팀은 시냅스 단백질 돌연변이 생쥐모델을 이용해 시냅스 단백질 속 네 개의 아미노산으로 이뤄진 작은 유전자 조각이 생후 생존율과 뇌 회로의 안정을 결정짓는 요인임을 밝혔다고 22일 설명했다.
시냅스 접착 단백질은 시냅스에 존재하며 시냅스의 형성, 유지, 가소성 등을 조절한다.
시냅스 접착 단백질 중 전시냅스에 존재하는 PTPδ(Protein Tyrosine Phosphatase delta)는 자폐스펙트럼장애, 주의력결핍과잉행동장애(ADHD), 강박장애, 하지불안증후군 등 여러 뇌 신경계 질환과 연관돼 있다.
특히 PTPδ의 경우, 특정 엑손(exon)의 선택적 스플라이싱(alternative splicing)이 시냅스 간 분자적 상호작용을 변화시킴으로써 시냅스 조절에 기여한다고 예측됐다. 하지만 유전자 변형 동물 모델을 이용한 실험을 통해 확인되지는 않았었다.
우선 연구진은 PTPδ의 작은 유전자 조각인 미니 엑손 B(mini-exon B)의 분자생물학적 기능을 밝히고자 미니 엑손 B가 결여될 경우 어떤 현상이 일어나는지 관찰했다. 미니 엑손 B가 완전히 결손된 새끼 쥐는 생후 생존율이 감소해 70% 이상이 사망했다.
미니 엑손 B가 일부만 결손되면 생존율에 영향은 없지만 성체가 되었을 때 불안 증세를 보였다.
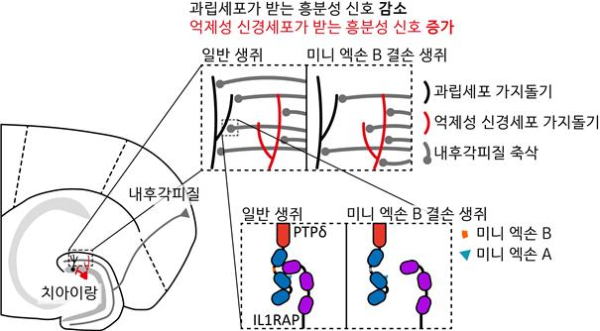
불안 증세가 나타나는 원인을 전기생리학 분석을 통해 살펴보니 미니 엑손 B가 결손되면 쥐의 해마 치아이랑(hippocampal dentate gyrus)에서 세포 유형별(과립세포, 억제성 신경세포)로 흥분성 시냅스의 수가 달라져 흥분-억제 비율이 망가짐을 확인했다.
과립세포가 받는 흥분성 신호는 감소하는 반면, 억제성 신경세포가 받는 흥분성 신호는 증가했다. 이는 뇌 신경회로의 흥분-억제 비율의 불균형을 일으켜, 실험 쥐가 밝거나 개방된 장소를 피하는 등 불안 증세를 보였다.
연구진은 시냅스 간 상호작용의 감소가 뇌 신경회로의 흥분-억제 비율의 불균형으로 이어진다는 점을 확인했다.
단백체학 분석을 통해 PTPδ와 상호작용하는 여러 단백질 중 후시냅스에 있는 IL1RAP 단백질을 살펴보니, 미니 엑손 B가 결손되면 IL1RAP 단백질도 줄어들었다. 이는 미니 엑손 B 결손 시 PTPδ-IL1RAP 시냅스 간 상호작용이 감소함을 의미한다.
이뿐만 아니라 IL1RAP 결손 생쥐에서도 흥분-억제 비율의 불균형이 나타났다. 즉 PTPδ의 미니 엑손 B는 시냅스 간 상호작용을 조절함으로써 신경세포의 흥분-억제 비율을 조절한다는 것이다.
김은준 단장은 “이번 연구는 단 네 개의 아미노산으로 이뤄진 유전자 조각이 생존율과 신경회로의 균형에 결정적인 영향을 줄 수 있음을 보여준다”며 “스플라이싱 오류가 뇌에 어떻게 작용하는지를 규명함으로써 향후 뇌 신경계 질환 치료법 개발에 단초를 제공할 것으로 기대된다”고 밝혔다.


